Если нет антигена то да
Препараты разрабатываемые против ВГВ
Правила форума
Внимание! Все советы и рекомендации медицинского характера, полученные при обсуждении, не могут рассматриваться как руководство к действию без согласования с лечащим врачом! Это может нанести вред вашему здоровью!
Внимание! Все советы и рекомендации медицинского характера, полученные при обсуждении, не могут рассматриваться как руководство к действию без согласования с лечащим врачом! Это может нанести вред вашему здоровью!
- Sovok-59
- Гуру
- Сообщения: 91316
- Зарегистрирован: 25 ноя 2010 12:11
- Пол: ♂
- Гепатит: С ушел в минус
- Фиброз: F1
- Генотип: 1
- Город: Челябинск
- Благодарил (а): 2144 раза
- Поблагодарили: 9546 раз
Препараты разрабатываемые против ВГВ
 Мои журналы
Мои журналы описание 2 терапий
описание 2 терапий-
Крисс
- Новичок
- Сообщения: 8
- Зарегистрирован: 20 сен 2021 10:17
- Пол: ♀
- Гепатит: В
- Генотип: B
- Город: Москва
Препараты разрабатываемые против ВГВ
А антиген это что?
Ничего не понимаю((
Столько маркеров, терминов((
Ничего не понимаю((
Столько маркеров, терминов((
- BigSlick
- Новичок
- Сообщения: 161
- Зарегистрирован: 18 авг 2016 17:50
- Пол: ♂
- Гепатит: В
- Генотип: D
- Город: Гражданин мира
- Благодарил (а): 4 раза
- Поблагодарили: 13 раз
Препараты разрабатываемые против ВГВ
Садиться на пегилированный интерферон на полгода такооое себе удовольствие.... Больше приобретешь, чем вылечишь.
- Scrooge805
- Местный
- Сообщения: 758
- Зарегистрирован: 16 фев 2019 05:32
- Пол: ♂
- Гепатит: В
- Фиброз: F0
- Генотип: A
- Город: Мск
- Благодарил (а): 139 раз
- Поблагодарили: 160 раз
Препараты разрабатываемые против ВГВ
как вы читаете на таком сайте исследования? Где искать методику и стадию?
Подробное описание:
Во время скринингового / базового визита (визит 1 / день 1), который совпадает с визитом 8 / день 43 начального исследования, подходящие пациенты будут получать открытый люматеперон 42 мг один раз в день в течение примерно 26 недель. Пациенты продолжат фоновую АДТ из начального исследования. Пациенты будут посещать еженедельно в течение 5 визита в неделю 4. В дальнейшем визиты будут происходить каждые две недели. Контрольный визит по вопросам безопасности будет проводиться во время посещения 17 / день 197, примерно через 2 недели после последней открытой дозы 42 мг люматеперона.
 скруджПВТ
скруджПВТ-
kriosan
- Бывалый
- Сообщения: 1578
- Зарегистрирован: 28 окт 2017 17:27
- Пол: ♂
- Гепатит: В
- Генотип: не определял(а)
- Город: Россия
- Благодарил (а): 566 раз
- Поблагодарили: 204 раза
Препараты разрабатываемые против ВГВ
Тоже никогда не понимал, как там инфа выложена.
Но как я понимаю, учитывая домен .gov, это какие-то государственные отчёты о планах и текущем ходе. Те не классические пресс-релизы
- Scrooge805
- Местный
- Сообщения: 758
- Зарегистрирован: 16 фев 2019 05:32
- Пол: ♂
- Гепатит: В
- Фиброз: F0
- Генотип: A
- Город: Мск
- Благодарил (а): 139 раз
- Поблагодарили: 160 раз
Препараты разрабатываемые против ВГВ
Жизненный цикл вируса гепатита В и цели лечения
Вирус гепатита B связывается с рецептором NTCP на поверхности клетки печени-хозяина через HBsAg, транспортирует нуклеокапсид вирусных частиц без оболочки к ядру, высвобождает двухцепочечную релаксированную кольцевую ДНК (ркДНК) и под действием ДНК-полимеразы превращает их в ковалентно замкнутые кольцевые суперспиральная ДНК (cccDNA). кскДНК имеет высокую степень стабильности и может сохраняться в ядре от месяцев до лет. Это ядро репликации вируса и инфицирования клеток. Вирус использует кзкДНК для транскрипции прегеномной РНК (пгРНК). пгРНК может осуществлять обратную транскрипцию ркДНК с образованием новых вирусных частиц. Зрелый нуклеокапсид либо циркулирует обратно в ядро для поддержания пула кзкДНК, либо упаковывается с белком оболочки и экспортируется в виде инфекционных вирусных частиц. 【2】
Соответственно, мишени гепатита B включают инвазию вируса, кзкДНК, мРНК вируса, сборку нуклеокапсида, упаковку и выделение вируса, а также иммунную регуляцию.

Существующие методы лечения гепатита B подавляют, но не могут уничтожить вирус. Лекарство пользуется большим спросом.
В настоящее время на рынке представлены в основном препараты от гепатита В двух типов: аналоги нуклеозидов (кислот) (НА) и интерферон. В настоящее время препараты NA широко используются в клинической практике. NA ингибирует вирусную полимеразу, конкурируя с природными нуклеозидами, чтобы блокировать синтез вирусных нуклеиновых кислот. Интерферон относительно дороже, требует внутримышечных инъекций и вызывает множество побочных реакций, поэтому его рынок постепенно сокращается.
Обычные лекарственные средства против гепатита В с НА в основном включают энтекавир, адефовир дипивоксил, ламивудин, телбивудин, тенофовир и т. Д. Благодаря превосходной безопасности и переносимости энтекавира и тенофовира, они включены в список препаратов первой линии для лечения гепатита B в соответствии с «последними рекомендациями по гепатиту B EASL (Европейское общество исследований печени) 2017 года», занимая огромную долю рынка в международные препараты против вируса гепатита В.
Препараты NA также являются основными лекарствами в Китае, на них приходится около 80% рынка лекарств от гепатита B. С 2012 по 2017 год CFDA одобрило 47 препаратов против гепатита В, в том числе 6 ламивудин, 20 адефовир, 13 энтекавир, 1 телбивудин и 6 тенофовир.
Особняком стоит доля рынка Энтекавира. В 2016 году общий внутренний рынок лекарств от вируса гепатита В в Китае достиг 16,2 миллиарда юаней. Он занимает половину доли рынка и стал основным продуктом отечественных противовирусных препаратов NA.
Многие китайские фармацевтические компании прошли «оценку устойчивости дженериков» для энтекавира. В тройку ведущих брендов энтекавира входят Runzhong от Chiatai Tianquing, Boluding от Bristol Myers Squibb и Weiliqing от Jiangxi Qingfeng Pharmaceutical. 【3】
Тенофовир - это продукт, разработанный компанией Gilead, которая недавно была запущена в Китае. Хотя его текущая доля невелика, перспективы быстрого роста многообещающие. В настоящее время многие отечественные фармацевтические компании, такие как Brilliant Pharmaceutical в Чэнду, прошли оценку согласованности, которая неизбежно приведет к перестройке внутреннего рынка. 【4】 Рыночные доли телбивудина, ламивудина и адефовира дипивоксила постепенно сокращаются из-за ограничения их безопасности и переносимости.

Зарубежные продажи основных препаратов против гепатита В
Однако и интерферон, и NA по-прежнему остаются в категории ингибирования репликации HBV, но не излечивают ее. Кроме того, очень высока вероятность рецидива через короткий промежуток времени после прекращения приема препарата.

Продажи лекарств против гепатита В в Китае в 2016 г.
Как сказал Х. Келли Райли, главный медицинский директор EnvisionRxOptions, текущее лечение гепатита B противовирусными препаратами в основном направлено на уменьшение повреждения печени и продление выживаемости пациентов, и может потребоваться пожизненное лекарственное лечение. Поэтому неизбежна разработка более эффективных лекарств для лечения хронического гепатита B.
Исследования и разработка новых лекарств от гепатита В
По сравнению с энергичной разработкой противовирусных препаратов от СПИДа и гепатита С, лекарствам от гепатита В не уделялось такого же внимания. За последние три десятилетия только около 10% всех противовирусных препаратов получили одобрение FDA для лечения гепатита B.
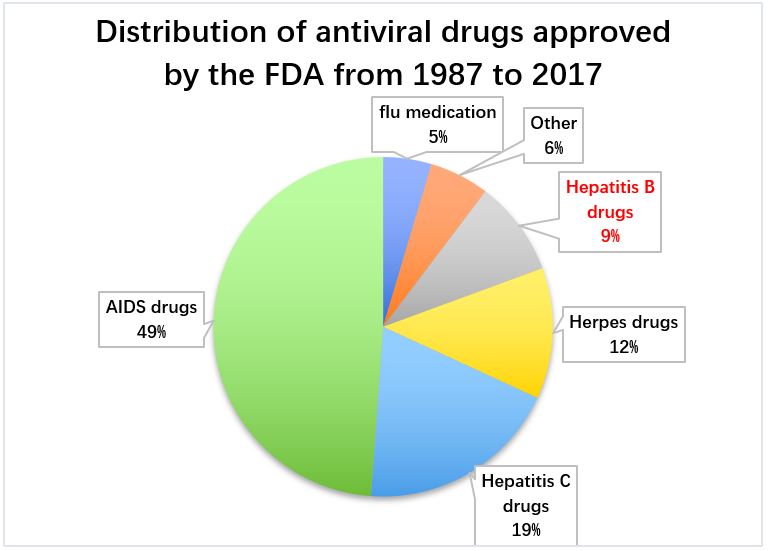
Распространение противовирусных препаратов, одобренных FDA с 1987 по 2017 гг.
В последние годы, с развитием технологии противовирусных препаратов, эпоха излечения гепатита B, кажется, становится реальной. Опираясь на огромный рыночный потенциал, в битву вступили крупные фармацевтические компании.
Горячие исследовательские препараты в настоящее время сосредоточены в следующих категориях: ингибиторы капсида, препараты РНКи и антисмысловой РНК, ингибиторы проникновения и терапевтические вакцины. Среди них ингибиторы капсида, препараты РНКи и антисмысловой РНК, а также терапевтические вакцины являются наиболее популярными направлениями разработки новых препаратов против гепатита В.
РНКи и антисмысловые РНК препараты
РНК-интерференция (РНКи) относится к случаю, когда молекулы РНК подавляют экспрессию или трансляцию генов, нейтрализуя целевые молекулы мРНК. Антисмысловая РНК относится к РНК, которая может ингибировать экспрессию родственных генов, будучи комплементарной мРНК. В настоящее время многие фармацевтические компании используют технологию РНКи и антисмысловой РНК для разработки лекарств для лечения хронического гепатита В.
Несколько международных гигантов, таких как Johnson & Johnson, GlaxoSmithKline и Roche, уже сотрудничают с другими фармацевтическими компаниями в разработке препаратов для РНКи и антисмысловой РНК. В настоящее время клинические испытания этих компаний вступили в позднюю стадию разработки. Для сравнения, отечественные китайские фармацевтические компании начали медленно, и в настоящее время игроков в этой категории меньше. Внимания заслуживают Brii Biosciences и Staidson.

Прогресс исследований препаратов против гепатита В с РНКи и антисмысловой РНК.
Примечание: Brii Biosciences (腾 盛 博 药), Staidson (舒泰 神), Johnson & Johnson (强 生)
1. Джонсон и Джонсон и Arrowhead: JNJ-3989
JNJ-3989 - это противовирусный препарат, вводимый подкожно, который предназначен для лечения хронического гепатита B с помощью РНКи. На только что завершившемся Европейском обществе по изучению заболеваний печени (EASL2020) Arrowhead и его партнер Johnson & Johnson обнародовали клинические данные фазы II двойной терапии JNJ-3989 и NA для лечения хронического гепатита B.
Результаты показали, что в течение 48 недель после последнего введения JNJ-3989 у 39% пациентов наблюдалось стойкое улучшение (падение HBsAg ≥1 log10IU / мл). У всех участников наблюдалось снижение уровня РНК HBV, HBeAg и HBcrAg. Показано, что один раз каждые 4 недели в общей сложности 3 дозы JNJ-3989 в дозе 400 мг имеют долгосрочную безопасность. Эти результаты подтверждают оценку большей продолжительности лечения комбинированной терапией JNJ-3989 + NA. 【6】
В то же время клинические испытания фазы 2 JNJ-3989, JNJ-6379 (еще один разрабатываемый препарат от гепатита B Johnson & Johnson) и тройной терапии NA. JNJ-6379 - это ингибитор капсида, который нарушает жизненный цикл HBV, вызывая сборку дефектных капсидов. JNJ-3989, JNJ-6379 и NA имеют разные цели. Ожидается, что комбинированное использование этих трех препаратов позволит сдерживать ВГВ на различных стадиях.

Лечение JNJ-3989
2. Ионис и GlaxoSmithKline: GlaxoSmithKline 3228836
В августе 2020 года антисмысловой препарат против гепатита B GlaxoSmithKline 3228836, совместно разработанный Ionis и GlaxoSmithKline, также объявил о своих клинических результатах 2 фазы. Было показано, что по сравнению с плацебо GlaxoSmithKline 3228836 снижает два биомаркера хронического гепатита B после 4 недель лечения: HBsAg и HBV.
В испытании участвовали четыре пациента с гепатитом B, которые ранее получали противовирусные препараты, и двенадцать пациентов с гепатитом B, которые не получали препараты от гепатита B. У шести пациентов в двух группах уровень HBsAg снизился на 3,0 log10 МЕ / мл или более через 29 дней.
Хотя результаты все еще находятся на предварительной стадии, Кристофер Корсико, старший вице-президент GlaxoSmithKline, сказал: «Результаты исследования являются потенциальным шагом к функциональной терапии пациентов с хроническим гепатитом В.» Клинические испытания фазы IIb начнутся до конца года. 【7】
3. Дисерна и Рош: RG6346
RG6346 - это препарат РНКи против гепатита В, разработанный совместно Dicerna и Roche. В модели HBV мыши RG6346 снижал циркулирующий HBsAg более чем на 99,9%. Это, по-видимому, указывает на то, что соединение может привести к долгосрочному клиренсу HBsAg.
В продолжающемся клиническом испытании фазы 1, подтверждающем концепцию, HBsAg в RG6346 в группах введения 1,5, 3,0 и 6,0 мг / кг был снижен до 1,39, 1,80 и 1,84 log10 МЕ / мл, соответственно, без возникновения побочных реакций.
4. Vir, Alnylam и Brii Biosciences: VIR-2218.
VIR-2218 представляет собой подкожную инъекцию РНКи для функционального лечения хронического гепатита B. VIR-2218 предназначен для подавления всей кзкДНК всех 10 генотипов HBV и всех транскриптов HBV в интегрированной ДНК. В настоящее время Brii Biosciences подала клиническую заявку на VIR-2218.
На EASL2020 Vir и Alnylam предоставили данные фазы II исследования VIR-2218 у пациентов с хроническим гепатитом B. В исследование были включены пациенты с гепатитом B, которые лечились с помощью NA, и результаты показали, что в продолжающемся исследовании с участием 24 пациентов с хронический гепатит В, нежелательных явлений не было. Кроме того, уровни HBsAg были значительно снижены во всех дозированных группах. Среди пациентов, получавших дозу 50 мг, уровень HBsAg больше всего снизился на 12-й неделе, в среднем на 1,5 log10 МЕ / мл по сравнению с исходным уровнем. Стоит отметить, что в этой группе снижение HBsAg все еще составляло 1,0 log10IU / мл до 28 недели. 【8】
5. Стайдсон: STSG-0002
Инъекция STSG-0002 - это лекарство от гепатита B, независимо разработанное Staidson в Пекине для блокирования репликации вируса HBV через механизм RNAi. В доклиническом исследовании эффективности с использованием модели трансгенных мышей HBV инъекция STSG-0002 показала значительный ингибирующий эффект на ДНК HBV через семь дней после введения. В сравнительном эксперименте с энтекавиром наблюдалось значительное снижение сывороточных HBsAg и HBeAg на следующий день после инъекции STSG-0002, в то время как HBsAg и HBeAg в группе энтекавира существенно не отличались от контрольной группы.
Чуваки, пока что вот так вылаживаю перевод с вышестоящего источника. Не полностью конечно, но будет время займусь остальным.
Из первой картинки понятно что есть 3 методики (направления) лечения HBV, выделил красным.
1. NUCs (ингибиторы энетекавир, тенофовир итд)
2. CpAM (какие то чудомолекулы)
3. РНК взломщики.
4. Ну и ИНТЕРФЕРОН, незнаю куда его нарисовать и вставить стрелкой, помоему он снаружи клетки должен быть))
какие то сомнения про VIR, почему к этому препарату привязались КИТАЙЦЫ? Никогда не стоит им доверять же, пословица гласит)). Если у меня на обычном интерфероне упало с 18000 до 800 это сколько log10будет? , примерно 1,3log10?
Вирус гепатита B связывается с рецептором NTCP на поверхности клетки печени-хозяина через HBsAg, транспортирует нуклеокапсид вирусных частиц без оболочки к ядру, высвобождает двухцепочечную релаксированную кольцевую ДНК (ркДНК) и под действием ДНК-полимеразы превращает их в ковалентно замкнутые кольцевые суперспиральная ДНК (cccDNA). кскДНК имеет высокую степень стабильности и может сохраняться в ядре от месяцев до лет. Это ядро репликации вируса и инфицирования клеток. Вирус использует кзкДНК для транскрипции прегеномной РНК (пгРНК). пгРНК может осуществлять обратную транскрипцию ркДНК с образованием новых вирусных частиц. Зрелый нуклеокапсид либо циркулирует обратно в ядро для поддержания пула кзкДНК, либо упаковывается с белком оболочки и экспортируется в виде инфекционных вирусных частиц. 【2】
Соответственно, мишени гепатита B включают инвазию вируса, кзкДНК, мРНК вируса, сборку нуклеокапсида, упаковку и выделение вируса, а также иммунную регуляцию.

Существующие методы лечения гепатита B подавляют, но не могут уничтожить вирус. Лекарство пользуется большим спросом.
В настоящее время на рынке представлены в основном препараты от гепатита В двух типов: аналоги нуклеозидов (кислот) (НА) и интерферон. В настоящее время препараты NA широко используются в клинической практике. NA ингибирует вирусную полимеразу, конкурируя с природными нуклеозидами, чтобы блокировать синтез вирусных нуклеиновых кислот. Интерферон относительно дороже, требует внутримышечных инъекций и вызывает множество побочных реакций, поэтому его рынок постепенно сокращается.
Обычные лекарственные средства против гепатита В с НА в основном включают энтекавир, адефовир дипивоксил, ламивудин, телбивудин, тенофовир и т. Д. Благодаря превосходной безопасности и переносимости энтекавира и тенофовира, они включены в список препаратов первой линии для лечения гепатита B в соответствии с «последними рекомендациями по гепатиту B EASL (Европейское общество исследований печени) 2017 года», занимая огромную долю рынка в международные препараты против вируса гепатита В.
Препараты NA также являются основными лекарствами в Китае, на них приходится около 80% рынка лекарств от гепатита B. С 2012 по 2017 год CFDA одобрило 47 препаратов против гепатита В, в том числе 6 ламивудин, 20 адефовир, 13 энтекавир, 1 телбивудин и 6 тенофовир.
Особняком стоит доля рынка Энтекавира. В 2016 году общий внутренний рынок лекарств от вируса гепатита В в Китае достиг 16,2 миллиарда юаней. Он занимает половину доли рынка и стал основным продуктом отечественных противовирусных препаратов NA.
Многие китайские фармацевтические компании прошли «оценку устойчивости дженериков» для энтекавира. В тройку ведущих брендов энтекавира входят Runzhong от Chiatai Tianquing, Boluding от Bristol Myers Squibb и Weiliqing от Jiangxi Qingfeng Pharmaceutical. 【3】
Тенофовир - это продукт, разработанный компанией Gilead, которая недавно была запущена в Китае. Хотя его текущая доля невелика, перспективы быстрого роста многообещающие. В настоящее время многие отечественные фармацевтические компании, такие как Brilliant Pharmaceutical в Чэнду, прошли оценку согласованности, которая неизбежно приведет к перестройке внутреннего рынка. 【4】 Рыночные доли телбивудина, ламивудина и адефовира дипивоксила постепенно сокращаются из-за ограничения их безопасности и переносимости.

Зарубежные продажи основных препаратов против гепатита В
Однако и интерферон, и NA по-прежнему остаются в категории ингибирования репликации HBV, но не излечивают ее. Кроме того, очень высока вероятность рецидива через короткий промежуток времени после прекращения приема препарата.

Продажи лекарств против гепатита В в Китае в 2016 г.
Как сказал Х. Келли Райли, главный медицинский директор EnvisionRxOptions, текущее лечение гепатита B противовирусными препаратами в основном направлено на уменьшение повреждения печени и продление выживаемости пациентов, и может потребоваться пожизненное лекарственное лечение. Поэтому неизбежна разработка более эффективных лекарств для лечения хронического гепатита B.
Исследования и разработка новых лекарств от гепатита В
По сравнению с энергичной разработкой противовирусных препаратов от СПИДа и гепатита С, лекарствам от гепатита В не уделялось такого же внимания. За последние три десятилетия только около 10% всех противовирусных препаратов получили одобрение FDA для лечения гепатита B.

Распространение противовирусных препаратов, одобренных FDA с 1987 по 2017 гг.
В последние годы, с развитием технологии противовирусных препаратов, эпоха излечения гепатита B, кажется, становится реальной. Опираясь на огромный рыночный потенциал, в битву вступили крупные фармацевтические компании.
Горячие исследовательские препараты в настоящее время сосредоточены в следующих категориях: ингибиторы капсида, препараты РНКи и антисмысловой РНК, ингибиторы проникновения и терапевтические вакцины. Среди них ингибиторы капсида, препараты РНКи и антисмысловой РНК, а также терапевтические вакцины являются наиболее популярными направлениями разработки новых препаратов против гепатита В.
РНКи и антисмысловые РНК препараты
РНК-интерференция (РНКи) относится к случаю, когда молекулы РНК подавляют экспрессию или трансляцию генов, нейтрализуя целевые молекулы мРНК. Антисмысловая РНК относится к РНК, которая может ингибировать экспрессию родственных генов, будучи комплементарной мРНК. В настоящее время многие фармацевтические компании используют технологию РНКи и антисмысловой РНК для разработки лекарств для лечения хронического гепатита В.
Несколько международных гигантов, таких как Johnson & Johnson, GlaxoSmithKline и Roche, уже сотрудничают с другими фармацевтическими компаниями в разработке препаратов для РНКи и антисмысловой РНК. В настоящее время клинические испытания этих компаний вступили в позднюю стадию разработки. Для сравнения, отечественные китайские фармацевтические компании начали медленно, и в настоящее время игроков в этой категории меньше. Внимания заслуживают Brii Biosciences и Staidson.

Прогресс исследований препаратов против гепатита В с РНКи и антисмысловой РНК.
Примечание: Brii Biosciences (腾 盛 博 药), Staidson (舒泰 神), Johnson & Johnson (强 生)
1. Джонсон и Джонсон и Arrowhead: JNJ-3989
JNJ-3989 - это противовирусный препарат, вводимый подкожно, который предназначен для лечения хронического гепатита B с помощью РНКи. На только что завершившемся Европейском обществе по изучению заболеваний печени (EASL2020) Arrowhead и его партнер Johnson & Johnson обнародовали клинические данные фазы II двойной терапии JNJ-3989 и NA для лечения хронического гепатита B.
Результаты показали, что в течение 48 недель после последнего введения JNJ-3989 у 39% пациентов наблюдалось стойкое улучшение (падение HBsAg ≥1 log10IU / мл). У всех участников наблюдалось снижение уровня РНК HBV, HBeAg и HBcrAg. Показано, что один раз каждые 4 недели в общей сложности 3 дозы JNJ-3989 в дозе 400 мг имеют долгосрочную безопасность. Эти результаты подтверждают оценку большей продолжительности лечения комбинированной терапией JNJ-3989 + NA. 【6】
В то же время клинические испытания фазы 2 JNJ-3989, JNJ-6379 (еще один разрабатываемый препарат от гепатита B Johnson & Johnson) и тройной терапии NA. JNJ-6379 - это ингибитор капсида, который нарушает жизненный цикл HBV, вызывая сборку дефектных капсидов. JNJ-3989, JNJ-6379 и NA имеют разные цели. Ожидается, что комбинированное использование этих трех препаратов позволит сдерживать ВГВ на различных стадиях.

Лечение JNJ-3989
2. Ионис и GlaxoSmithKline: GlaxoSmithKline 3228836
В августе 2020 года антисмысловой препарат против гепатита B GlaxoSmithKline 3228836, совместно разработанный Ionis и GlaxoSmithKline, также объявил о своих клинических результатах 2 фазы. Было показано, что по сравнению с плацебо GlaxoSmithKline 3228836 снижает два биомаркера хронического гепатита B после 4 недель лечения: HBsAg и HBV.
В испытании участвовали четыре пациента с гепатитом B, которые ранее получали противовирусные препараты, и двенадцать пациентов с гепатитом B, которые не получали препараты от гепатита B. У шести пациентов в двух группах уровень HBsAg снизился на 3,0 log10 МЕ / мл или более через 29 дней.
Хотя результаты все еще находятся на предварительной стадии, Кристофер Корсико, старший вице-президент GlaxoSmithKline, сказал: «Результаты исследования являются потенциальным шагом к функциональной терапии пациентов с хроническим гепатитом В.» Клинические испытания фазы IIb начнутся до конца года. 【7】
3. Дисерна и Рош: RG6346
RG6346 - это препарат РНКи против гепатита В, разработанный совместно Dicerna и Roche. В модели HBV мыши RG6346 снижал циркулирующий HBsAg более чем на 99,9%. Это, по-видимому, указывает на то, что соединение может привести к долгосрочному клиренсу HBsAg.
В продолжающемся клиническом испытании фазы 1, подтверждающем концепцию, HBsAg в RG6346 в группах введения 1,5, 3,0 и 6,0 мг / кг был снижен до 1,39, 1,80 и 1,84 log10 МЕ / мл, соответственно, без возникновения побочных реакций.
4. Vir, Alnylam и Brii Biosciences: VIR-2218.
VIR-2218 представляет собой подкожную инъекцию РНКи для функционального лечения хронического гепатита B. VIR-2218 предназначен для подавления всей кзкДНК всех 10 генотипов HBV и всех транскриптов HBV в интегрированной ДНК. В настоящее время Brii Biosciences подала клиническую заявку на VIR-2218.
На EASL2020 Vir и Alnylam предоставили данные фазы II исследования VIR-2218 у пациентов с хроническим гепатитом B. В исследование были включены пациенты с гепатитом B, которые лечились с помощью NA, и результаты показали, что в продолжающемся исследовании с участием 24 пациентов с хронический гепатит В, нежелательных явлений не было. Кроме того, уровни HBsAg были значительно снижены во всех дозированных группах. Среди пациентов, получавших дозу 50 мг, уровень HBsAg больше всего снизился на 12-й неделе, в среднем на 1,5 log10 МЕ / мл по сравнению с исходным уровнем. Стоит отметить, что в этой группе снижение HBsAg все еще составляло 1,0 log10IU / мл до 28 недели. 【8】
5. Стайдсон: STSG-0002
Инъекция STSG-0002 - это лекарство от гепатита B, независимо разработанное Staidson в Пекине для блокирования репликации вируса HBV через механизм RNAi. В доклиническом исследовании эффективности с использованием модели трансгенных мышей HBV инъекция STSG-0002 показала значительный ингибирующий эффект на ДНК HBV через семь дней после введения. В сравнительном эксперименте с энтекавиром наблюдалось значительное снижение сывороточных HBsAg и HBeAg на следующий день после инъекции STSG-0002, в то время как HBsAg и HBeAg в группе энтекавира существенно не отличались от контрольной группы.
Чуваки, пока что вот так вылаживаю перевод с вышестоящего источника. Не полностью конечно, но будет время займусь остальным.
Из первой картинки понятно что есть 3 методики (направления) лечения HBV, выделил красным.
1. NUCs (ингибиторы энетекавир, тенофовир итд)
2. CpAM (какие то чудомолекулы)
3. РНК взломщики.
4. Ну и ИНТЕРФЕРОН, незнаю куда его нарисовать и вставить стрелкой, помоему он снаружи клетки должен быть))
какие то сомнения про VIR, почему к этому препарату привязались КИТАЙЦЫ? Никогда не стоит им доверять же, пословица гласит)). Если у меня на обычном интерфероне упало с 18000 до 800 это сколько log10будет? , примерно 1,3log10?
 скруджПВТ
скруджПВТ-
Крисс
- Новичок
- Сообщения: 8
- Зарегистрирован: 20 сен 2021 10:17
- Пол: ♀
- Гепатит: В
- Генотип: B
- Город: Москва
Препараты разрабатываемые против ВГВ
Вирус сидит в гепаците. Значит нужно убить Вирус с больным гепацитом? Нужно лекарство которое соединяется также как и Вирус и уничтожает уже заражённые местечки?
-
Busan
- Новичок
- Сообщения: 158
- Зарегистрирован: 14 ноя 2018 11:56
- Пол: ♂
- Гепатит: Гепатита нет
- Генотип: не определял(а)
- Город: Busan
- Благодарил (а): 9 раз
- Поблагодарили: 31 раз
Препараты разрабатываемые против ВГВ
Такое может делать только клетка Т-киллер, он находит заражённую клетку и отдаёт приказ ей на самоуничтожение или выделяет перфорины которые продырявливают мембрану клетки. Вызов это как нацелит их на заражённые клетки
- Scrooge805
- Местный
- Сообщения: 758
- Зарегистрирован: 16 фев 2019 05:32
- Пол: ♂
- Гепатит: В
- Фиброз: F0
- Генотип: A
- Город: Мск
- Благодарил (а): 139 раз
- Поблагодарили: 160 раз
Препараты разрабатываемые против ВГВ
https://ru.wikipedia.org/wiki/%D0%92%D0 ... 0%B3%D0%B8
Кто нибудь копал тему вирофагов?
Вирофа́ги[2][3] (англ. Virophages, лат. Lavidaviridae) — группа вирусов, которые могут размножаться в клетках только в присутствии другого вируса (вируса-хозяина), однако имеющих более сложные геномы и вирионы, чем другие вирусы-сателлиты[4]. Вирофаги имеют икосаэдрические капсиды, их геномы представлены двуцепочечными молекулами ДНК. Первые представители этой группы вирусов описаны в 2008 году, и к концу 2016 года было известно 18 геномов вирофагов, два из которых почти полностью секвенированы. Вирофаги обнаружены в самых разных местообитаниях — в глубоководных районах океанов и на суше; один вирофаг был выделен из жидкости для контактных линз, поэтому, возможно, вирофаги взаимодействуют и с организмом человека[5].
Вирофагов предложено выделять в семейство Lavidaviridae, филогенетические связи которого пока не вполне выяснены[5][6]. Впрочем, по состоянию на март 2018 года Международный комитет по таксономии вирусов официально признавал только два рода и три вида[7]
Походу было бы круто если синтезируют такой вирофаг который размножается в антигене HBsAg, полностью заменит все частицы которые плавают в межклеточном пространстве на viroHBsAg и тесты не будут определять их как гепатитные. Возможно в будущем придумают вирус для вируса, так может проще чем идти по линии иммунной системы?
Кто нибудь копал тему вирофагов?
Вирофа́ги[2][3] (англ. Virophages, лат. Lavidaviridae) — группа вирусов, которые могут размножаться в клетках только в присутствии другого вируса (вируса-хозяина), однако имеющих более сложные геномы и вирионы, чем другие вирусы-сателлиты[4]. Вирофаги имеют икосаэдрические капсиды, их геномы представлены двуцепочечными молекулами ДНК. Первые представители этой группы вирусов описаны в 2008 году, и к концу 2016 года было известно 18 геномов вирофагов, два из которых почти полностью секвенированы. Вирофаги обнаружены в самых разных местообитаниях — в глубоководных районах океанов и на суше; один вирофаг был выделен из жидкости для контактных линз, поэтому, возможно, вирофаги взаимодействуют и с организмом человека[5].
Вирофагов предложено выделять в семейство Lavidaviridae, филогенетические связи которого пока не вполне выяснены[5][6]. Впрочем, по состоянию на март 2018 года Международный комитет по таксономии вирусов официально признавал только два рода и три вида[7]
Походу было бы круто если синтезируют такой вирофаг который размножается в антигене HBsAg, полностью заменит все частицы которые плавают в межклеточном пространстве на viroHBsAg и тесты не будут определять их как гепатитные. Возможно в будущем придумают вирус для вируса, так может проще чем идти по линии иммунной системы?
 скруджПВТ
скруджПВТ-
kriosan
- Бывалый
- Сообщения: 1578
- Зарегистрирован: 28 окт 2017 17:27
- Пол: ♂
- Гепатит: В
- Генотип: не определял(а)
- Город: Россия
- Благодарил (а): 566 раз
- Поблагодарили: 204 раза
-
kriosan
- Бывалый
- Сообщения: 1578
- Зарегистрирован: 28 окт 2017 17:27
- Пол: ♂
- Гепатит: В
- Генотип: не определял(а)
- Город: Россия
- Благодарил (а): 566 раз
- Поблагодарили: 204 раза
Препараты разрабатываемые против ВГВ
Привет) Я вспомнил, кого мне напомнил твой ник)
Почитай отзыв о Бараклюде на сайте
https://otzyvy.pro/reviews/otzyvy-entekavir-157021.html
Это не ты, тот самый Нико?
- Scrooge805
- Местный
- Сообщения: 758
- Зарегистрирован: 16 фев 2019 05:32
- Пол: ♂
- Гепатит: В
- Фиброз: F0
- Генотип: A
- Город: Мск
- Благодарил (а): 139 раз
- Поблагодарили: 160 раз
Препараты разрабатываемые против ВГВ
На ILC 2021 объявлено об успехах в разработке новых препаратов для лечения гепатита B и D
Ведущие исследователи-гепатологи объявили сегодня на Международном конгрессе по печени 2021 г. о важных новых разработках в области исследования гепатита.
Сюда входят новые данные о противовирусных препаратах для лечения гепатита B и D, а также о применении инфузионной химиотерапии с ингибиторами P-1 для лечения рака печени.
Другие объявления включали обзор воздействия пандемии COVID-19 на усилия по ликвидации гепатита С в США и некоторые обнадеживающие данные испытания нового устройства для диализа печени для лечения острой хронической печеночной недостаточности (ACLF).
«Ученые и правозащитники давно утверждают, что если мы реально собираемся ликвидировать гепатит B, то нам потребуется функциональное лечение», - сказал Филип Ньюсом, генеральный секретарь EASL и профессор экспериментальной гепатологии и директор Центра исследований печени в Бирмингемский университет в Великобритании. «Результаты испытаний терапевтического препарата RNAi VIR-2218 являются обнадеживающим примером того, что излечение возможно раньше, чем позже, с потенциальными последствиями в реальном мире для 300 миллионов человек, живущих с этим заболеванием».
Каждый год 30 миллионов человек заражаются гепатитом B, и, по оценкам, 884 000 человек ежегодно умирают от этого заболевания и связанных с ним осложнений, таких как рак печени. На сегодняшней официальной пресс-конференции было освещено пять исследований, охватывающих исследования по лечению и лечению гепатита и острой хронической печеночной недостаточности, отобранных из более чем 1500 тезисов, представленных на ILC 2021.
Влияние COVID-19 на элиминацию гепатита (ВГС) в США.
По состоянию на 2019 год Соединенные Штаты (США) не смогли достичь целей ВОЗ по элиминации из-за роста заболеваемости и препятствий на пути к лечению. В 2020 году пандемия COVID-19 нарушила работу служб по лечению ВГС во всем мире: на лечение начали на 25 процентов меньше пациентов, чем в 2019 году. Исследователи обновили ранее утвержденную модель Маркова для оценки заболеваемости и смертности от ВГС в США. Были разработаны три сценария для оценки возможных результатов восстановления ВГС после пандемии. К ним относятся: 1) длительные сбои в лечении; 2) вернуться к прогнозам лечения до COVID-19; 3) Достичь целей ВОЗ за счет усиления лечения и снижения вреда.
Сара Блах из Фонда CDA в США сообщила, что в период с 2014 по 2019 гг. Около 1,2 миллиона пациентов прошли курс лечения от ВГС, что привело к более чем 50% сокращению случаев гепатоцеллюлярной карциномы (ГЦК) и более чем 65% снижению смертности, связанной с ВГС, связанной с печенью ( LRD) в 2019 году по сравнению с 2014 годом. В смоделированных сценариях от 780 000 до 2,3 миллиона пациентов (в совокупности) будут начаты лечение в период с 2021 по 2030 год. Цели ВОЗ (сценарий 3) могут быть достигнуты в США за счет лечения не менее 240 000 пациентов в год и расширения доступа к программам снижения вреда. По сравнению со сценарием 1, сценарии 2 и 3 могут предотвратить 19 400 случаев LRD и 9 500 случаев HCC и 33 200 случаев LRD и 24 900 случаев HCC соответственно. Резюме: Моделирование восстановления элиминации ВГС после пандемии COVID-19 в США: пути восстановления прогресса (LBP-2814)
Терапевтический противовирусный препарат РНКи VIR-2218 перспективен для пациентов с хронической инфекцией гепатита В.
VIR-2218 представляет собой исследуемый GalNAc-конъюгированную малую интерферирующую рибонуклеиновую кислоту (миРНК) терапевтический препарат, который разрабатывается для функционального лечения хронической вирусной инфекции гепатита В (ХГВ). VIR-2218 был создан с использованием Enhanced Stabilization Chemistry Plus, который сохраняет активность in vivo при одновременном снижении побочных эффектов. VIR-2218 нацелен на консервативную область гена X и предназначен для подавления всех основных транскриптов HBV, как из кзкДНК, так и из интегрированной ДНК, по всем 10 генотипам HBV в виде единой миРНК.
Эд Гейн из Оклендского университета в Новой Зеландии сообщил, что две дозы VIR-2218 по 20-200 мг с интервалом в 4 недели хорошо переносились участниками ХГВ.
Существенное снижение HBsAg наблюдалось как у участников HBeAg-, так и у HBeAg + при всех уровнях доз, что позволяет предположить, что VIR-2218 может заглушать транскрипты как кзкДНК, так и интегрированной ДНК. Противовирусная активность VIR-2218, продемонстрированная в этом исследовании, поддерживает дальнейшее развитие в рамках комбинированных схем, направленных на функциональное излечение. Резюме: Безопасность и противовирусная активность VIR-2218, препарата X-нацеленной РНКи, у участников с хронической инфекцией гепатита B: результаты наблюдения 48 недели (OA-44)
Обнадеживающие промежуточные данные фазы III исследования монотерапии противовирусным препаратом булевиртидом у пациентов с хроническим гепатитом дельта/
Булевиртид (BLV) является первым в своем классе ингибитором для лечения хронической инфекции вируса гепатита D (HDV). BLV показал выраженный вирусологический и биохимический ответ (снижение РНК HDV и ALT) в двух испытаниях фазы 2 (MYR202 / MYR203). В этом исследовании представлены обнадеживающие данные предварительно определенного 24-недельного промежуточного анализа исследования MYR301 фазы 3 у пациентов с коинфекцией HBV / HDV, получающих монотерапию BLV в дозе 2 мг / день или 10 мг / день в сутки, по сравнению с наблюдением без противовирусного лечения (всего 150 пациенты).
Хайнер Ведемайер из Ганноверской медицинской больницы в Германии отметил, что после 24 недель исследований это исследование фазы 3 подтверждает, что монотерапия BLV безопасна и хорошо переносится пациентами с компенсированным дельта-гепатитом. 24 недели лечения BLV были связаны со значительным снижением РНК HDV и улучшением биохимической активности заболевания. Он пришел к выводу, что эти результаты подтверждают условное одобрение BLV. Резюме: Монотерапия булевиртидом в низкой и высокой дозе у пациентов с хроническим гепатитом дельта: промежуточные данные за 24 недели исследования фазы 3 MYR301 (LBP-2730)
Инфузионная химиотерапия в сочетании с синтилимабом может помочь вылечить рак печени
Это исследование было направлено на изучение эффективности и безопасности химиотерапии инфузией печеночной артерии в сочетании с синтилимабом (ингибитор PD-1) при местно-распространенном потенциально операбельном ГЦК. Всего было включено 30 пациентов со средним возрастом 50,5 лет (диапазон 34-70), 93,3% мужчин и 96,7% инфицированных HBV. Средний цикл лечения составлял 2 года. Оценка опухоли проводилась каждые 6-8 недель. Пациенты с уменьшением опухоли и подходящими для резекции R0 были направлены на гепатэктомию, затем продолжили монотерапию синтилимабом максимум на 16 курсов. Первичной конечной точкой была выживаемость без прогрессирования заболевания (ВБП) согласно RECIST 1.1, определяемая как время от первого дня лечения до прогрессирования заболевания, послеоперационного рецидива или смерти.
Ли Сюй из Онкологического центра Университета Сунь Ятсена в Китае объяснил, что по состоянию на апрель 2021 года 29 пациентов регулярно обследовались со средним сроком наблюдения 17,1 месяца (диапазон: 6,5-25,6). Медианы ВБП и ОВ не были достигнуты, а показатели ВБП и ОВ через 12 месяцев составили 57,6% (95% ДИ 41,9–79,2) и 82,3% (95% ДИ 69,4–97,1), соответственно. ЧОО и ДКР составили 44,8% (13/29) и 75,9% (22/29). 19 (65,5%) пациентов получили гепатэктомию с 3 патологическими полными ответами (pCR). Еще 2 пациента с глубоким ответом получили радикальную абляцию, и у 1 был подтвержден pCR с помощью игольной биопсии. У 14 пациентов пока нет опухолей. Большинство НЯ, связанных с лечением (TRAE), были 1-2 степени, наиболее частыми НЯ были гипертермия (10%), сыпь (10%) и зуд (10%). Только у 1 пациента наблюдалась обратимая иммунная дисфункция печени 4 степени. Никаких других TRAE или SAE 3-5 степени не наблюдалось. Химиотерапия инфузией печеночной артерии в сочетании с ингибитором PD-1 показала высокий коэффициент конверсии и хороший профиль безопасности. Комбинированная стратегия может рассматриваться как оптимальный вариант лечения, обеспечивающий шанс излечения местнораспространенного и потенциально операбельного ГЦК. Резюме: Инфузионная химиотерапия печеночной артерии в сочетании с ингибитором PD-1 в качестве конверсионной терапии при местнораспространенной потенциально резектабельной гепатоцеллюлярной карциноме: исследование фазы II (OA-2679) Сессия: пятница, 25 июня, 14: 00-15: 30
Новое устройство для диализа печени показывает обнадеживающие предварительные результаты в лечении острой или хронической печеночной недостаточности (ACLF)
Лечение острой хронической печеночной недостаточности (ACLF) является неудовлетворенной потребностью. В настоящее время стандарт медицинской помощи (SOC) включает лечение инфекций с помощью антибиотиков и поддержки отдельных органов, диализ при почечной недостаточности и прессоры при низком кровяном давлении. В настоящее время существует очень мало вариантов модификации болезни; стероиды могут играть роль в некоторых заболеваниях печени, но большая часть пациентов не реагирует на стероиды, а стероиды сопряжены с внутренним риском новых инфекций. Трансплантация печени - это вариант, но он недоступен в Великобритании для многих из этих пациентов.
Это рандомизированное исследование проверяет гипотезу о том, что DIALIVE, новое устройство для диализа печени, значительно улучшит прогноз пациентов с ACLF. Первичной конечной точкой была безопасность; производительность устройства; клинические и патофизиологические эффекты. DIALIVE в основном заменяет дисфункциональный альбумин и удаляет патогены и связанные с повреждениями молекулярные структуры.
Пациенты с 32-ACLF с алкогольным циррозом печени были рандомизированы в группы DIALIVE или SOC. Для оценки пациента потребовалось минимум 3 сеанса DIALIVE (максимум 5). Испытание проводилось на пациентах, поступивших в отделения интенсивной терапии с острым обострением хронического заболевания печени, которое быстро прогрессировало до серьезного дополнительного ухудшения функции печени и отказа других важных органов, таких как почки, мозг и легкие. .
Банвари Агарвал из Королевской бесплатной больницы в Великобритании отметил, что, хотя количество изученных пациентов относительно невелико, данные пока указывают на очень сильный сигнал, свидетельствующий о том, что пациенты, получавшие Dialive, имели значительно более высокую вероятность выздоровления от этого острого обострения и вернуться к уровню печени и других органов, который был до болезни. DIALIVE безопасен и значительно увеличивает долю пациентов, у которых разрешается ACLF, одновременно сокращая время до разрешения. Эти данные оправдывают начало клинических испытаний поздней фазы.
Агарвал добавил, что у Dialive есть два основных преимущества: а) он относительно прост в сборке и позволяет использовать оборудование, уже используемое в отделениях интенсивной терапии, и б) он нацелен на два важных патобиологических механизма, которые, как известно, вызывают резкое снижение функции печени и связанная с этим недостаточность других органов, а именно собственный поврежденный альбумин пациента и развитие интенсивной системной воспалительной реакции. Резюме:
Многоцентровое рандомизированное контролируемое исследование для оценки безопасности и эффективности устройства для диализа печени DIALIVE у пациентов с острой хронической печеночной недостаточностью (ACLF) по сравнению со стандартным лечением (SOC). (OA-1997)
Ведущие исследователи-гепатологи объявили сегодня на Международном конгрессе по печени 2021 г. о важных новых разработках в области исследования гепатита.
Сюда входят новые данные о противовирусных препаратах для лечения гепатита B и D, а также о применении инфузионной химиотерапии с ингибиторами P-1 для лечения рака печени.
Другие объявления включали обзор воздействия пандемии COVID-19 на усилия по ликвидации гепатита С в США и некоторые обнадеживающие данные испытания нового устройства для диализа печени для лечения острой хронической печеночной недостаточности (ACLF).
«Ученые и правозащитники давно утверждают, что если мы реально собираемся ликвидировать гепатит B, то нам потребуется функциональное лечение», - сказал Филип Ньюсом, генеральный секретарь EASL и профессор экспериментальной гепатологии и директор Центра исследований печени в Бирмингемский университет в Великобритании. «Результаты испытаний терапевтического препарата RNAi VIR-2218 являются обнадеживающим примером того, что излечение возможно раньше, чем позже, с потенциальными последствиями в реальном мире для 300 миллионов человек, живущих с этим заболеванием».
Каждый год 30 миллионов человек заражаются гепатитом B, и, по оценкам, 884 000 человек ежегодно умирают от этого заболевания и связанных с ним осложнений, таких как рак печени. На сегодняшней официальной пресс-конференции было освещено пять исследований, охватывающих исследования по лечению и лечению гепатита и острой хронической печеночной недостаточности, отобранных из более чем 1500 тезисов, представленных на ILC 2021.
Влияние COVID-19 на элиминацию гепатита (ВГС) в США.
По состоянию на 2019 год Соединенные Штаты (США) не смогли достичь целей ВОЗ по элиминации из-за роста заболеваемости и препятствий на пути к лечению. В 2020 году пандемия COVID-19 нарушила работу служб по лечению ВГС во всем мире: на лечение начали на 25 процентов меньше пациентов, чем в 2019 году. Исследователи обновили ранее утвержденную модель Маркова для оценки заболеваемости и смертности от ВГС в США. Были разработаны три сценария для оценки возможных результатов восстановления ВГС после пандемии. К ним относятся: 1) длительные сбои в лечении; 2) вернуться к прогнозам лечения до COVID-19; 3) Достичь целей ВОЗ за счет усиления лечения и снижения вреда.
Сара Блах из Фонда CDA в США сообщила, что в период с 2014 по 2019 гг. Около 1,2 миллиона пациентов прошли курс лечения от ВГС, что привело к более чем 50% сокращению случаев гепатоцеллюлярной карциномы (ГЦК) и более чем 65% снижению смертности, связанной с ВГС, связанной с печенью ( LRD) в 2019 году по сравнению с 2014 годом. В смоделированных сценариях от 780 000 до 2,3 миллиона пациентов (в совокупности) будут начаты лечение в период с 2021 по 2030 год. Цели ВОЗ (сценарий 3) могут быть достигнуты в США за счет лечения не менее 240 000 пациентов в год и расширения доступа к программам снижения вреда. По сравнению со сценарием 1, сценарии 2 и 3 могут предотвратить 19 400 случаев LRD и 9 500 случаев HCC и 33 200 случаев LRD и 24 900 случаев HCC соответственно. Резюме: Моделирование восстановления элиминации ВГС после пандемии COVID-19 в США: пути восстановления прогресса (LBP-2814)
Терапевтический противовирусный препарат РНКи VIR-2218 перспективен для пациентов с хронической инфекцией гепатита В.
VIR-2218 представляет собой исследуемый GalNAc-конъюгированную малую интерферирующую рибонуклеиновую кислоту (миРНК) терапевтический препарат, который разрабатывается для функционального лечения хронической вирусной инфекции гепатита В (ХГВ). VIR-2218 был создан с использованием Enhanced Stabilization Chemistry Plus, который сохраняет активность in vivo при одновременном снижении побочных эффектов. VIR-2218 нацелен на консервативную область гена X и предназначен для подавления всех основных транскриптов HBV, как из кзкДНК, так и из интегрированной ДНК, по всем 10 генотипам HBV в виде единой миРНК.
Эд Гейн из Оклендского университета в Новой Зеландии сообщил, что две дозы VIR-2218 по 20-200 мг с интервалом в 4 недели хорошо переносились участниками ХГВ.
Существенное снижение HBsAg наблюдалось как у участников HBeAg-, так и у HBeAg + при всех уровнях доз, что позволяет предположить, что VIR-2218 может заглушать транскрипты как кзкДНК, так и интегрированной ДНК. Противовирусная активность VIR-2218, продемонстрированная в этом исследовании, поддерживает дальнейшее развитие в рамках комбинированных схем, направленных на функциональное излечение. Резюме: Безопасность и противовирусная активность VIR-2218, препарата X-нацеленной РНКи, у участников с хронической инфекцией гепатита B: результаты наблюдения 48 недели (OA-44)
Обнадеживающие промежуточные данные фазы III исследования монотерапии противовирусным препаратом булевиртидом у пациентов с хроническим гепатитом дельта/
Булевиртид (BLV) является первым в своем классе ингибитором для лечения хронической инфекции вируса гепатита D (HDV). BLV показал выраженный вирусологический и биохимический ответ (снижение РНК HDV и ALT) в двух испытаниях фазы 2 (MYR202 / MYR203). В этом исследовании представлены обнадеживающие данные предварительно определенного 24-недельного промежуточного анализа исследования MYR301 фазы 3 у пациентов с коинфекцией HBV / HDV, получающих монотерапию BLV в дозе 2 мг / день или 10 мг / день в сутки, по сравнению с наблюдением без противовирусного лечения (всего 150 пациенты).
Хайнер Ведемайер из Ганноверской медицинской больницы в Германии отметил, что после 24 недель исследований это исследование фазы 3 подтверждает, что монотерапия BLV безопасна и хорошо переносится пациентами с компенсированным дельта-гепатитом. 24 недели лечения BLV были связаны со значительным снижением РНК HDV и улучшением биохимической активности заболевания. Он пришел к выводу, что эти результаты подтверждают условное одобрение BLV. Резюме: Монотерапия булевиртидом в низкой и высокой дозе у пациентов с хроническим гепатитом дельта: промежуточные данные за 24 недели исследования фазы 3 MYR301 (LBP-2730)
Инфузионная химиотерапия в сочетании с синтилимабом может помочь вылечить рак печени
Это исследование было направлено на изучение эффективности и безопасности химиотерапии инфузией печеночной артерии в сочетании с синтилимабом (ингибитор PD-1) при местно-распространенном потенциально операбельном ГЦК. Всего было включено 30 пациентов со средним возрастом 50,5 лет (диапазон 34-70), 93,3% мужчин и 96,7% инфицированных HBV. Средний цикл лечения составлял 2 года. Оценка опухоли проводилась каждые 6-8 недель. Пациенты с уменьшением опухоли и подходящими для резекции R0 были направлены на гепатэктомию, затем продолжили монотерапию синтилимабом максимум на 16 курсов. Первичной конечной точкой была выживаемость без прогрессирования заболевания (ВБП) согласно RECIST 1.1, определяемая как время от первого дня лечения до прогрессирования заболевания, послеоперационного рецидива или смерти.
Ли Сюй из Онкологического центра Университета Сунь Ятсена в Китае объяснил, что по состоянию на апрель 2021 года 29 пациентов регулярно обследовались со средним сроком наблюдения 17,1 месяца (диапазон: 6,5-25,6). Медианы ВБП и ОВ не были достигнуты, а показатели ВБП и ОВ через 12 месяцев составили 57,6% (95% ДИ 41,9–79,2) и 82,3% (95% ДИ 69,4–97,1), соответственно. ЧОО и ДКР составили 44,8% (13/29) и 75,9% (22/29). 19 (65,5%) пациентов получили гепатэктомию с 3 патологическими полными ответами (pCR). Еще 2 пациента с глубоким ответом получили радикальную абляцию, и у 1 был подтвержден pCR с помощью игольной биопсии. У 14 пациентов пока нет опухолей. Большинство НЯ, связанных с лечением (TRAE), были 1-2 степени, наиболее частыми НЯ были гипертермия (10%), сыпь (10%) и зуд (10%). Только у 1 пациента наблюдалась обратимая иммунная дисфункция печени 4 степени. Никаких других TRAE или SAE 3-5 степени не наблюдалось. Химиотерапия инфузией печеночной артерии в сочетании с ингибитором PD-1 показала высокий коэффициент конверсии и хороший профиль безопасности. Комбинированная стратегия может рассматриваться как оптимальный вариант лечения, обеспечивающий шанс излечения местнораспространенного и потенциально операбельного ГЦК. Резюме: Инфузионная химиотерапия печеночной артерии в сочетании с ингибитором PD-1 в качестве конверсионной терапии при местнораспространенной потенциально резектабельной гепатоцеллюлярной карциноме: исследование фазы II (OA-2679) Сессия: пятница, 25 июня, 14: 00-15: 30
Новое устройство для диализа печени показывает обнадеживающие предварительные результаты в лечении острой или хронической печеночной недостаточности (ACLF)
Лечение острой хронической печеночной недостаточности (ACLF) является неудовлетворенной потребностью. В настоящее время стандарт медицинской помощи (SOC) включает лечение инфекций с помощью антибиотиков и поддержки отдельных органов, диализ при почечной недостаточности и прессоры при низком кровяном давлении. В настоящее время существует очень мало вариантов модификации болезни; стероиды могут играть роль в некоторых заболеваниях печени, но большая часть пациентов не реагирует на стероиды, а стероиды сопряжены с внутренним риском новых инфекций. Трансплантация печени - это вариант, но он недоступен в Великобритании для многих из этих пациентов.
Это рандомизированное исследование проверяет гипотезу о том, что DIALIVE, новое устройство для диализа печени, значительно улучшит прогноз пациентов с ACLF. Первичной конечной точкой была безопасность; производительность устройства; клинические и патофизиологические эффекты. DIALIVE в основном заменяет дисфункциональный альбумин и удаляет патогены и связанные с повреждениями молекулярные структуры.
Пациенты с 32-ACLF с алкогольным циррозом печени были рандомизированы в группы DIALIVE или SOC. Для оценки пациента потребовалось минимум 3 сеанса DIALIVE (максимум 5). Испытание проводилось на пациентах, поступивших в отделения интенсивной терапии с острым обострением хронического заболевания печени, которое быстро прогрессировало до серьезного дополнительного ухудшения функции печени и отказа других важных органов, таких как почки, мозг и легкие. .
Банвари Агарвал из Королевской бесплатной больницы в Великобритании отметил, что, хотя количество изученных пациентов относительно невелико, данные пока указывают на очень сильный сигнал, свидетельствующий о том, что пациенты, получавшие Dialive, имели значительно более высокую вероятность выздоровления от этого острого обострения и вернуться к уровню печени и других органов, который был до болезни. DIALIVE безопасен и значительно увеличивает долю пациентов, у которых разрешается ACLF, одновременно сокращая время до разрешения. Эти данные оправдывают начало клинических испытаний поздней фазы.
Агарвал добавил, что у Dialive есть два основных преимущества: а) он относительно прост в сборке и позволяет использовать оборудование, уже используемое в отделениях интенсивной терапии, и б) он нацелен на два важных патобиологических механизма, которые, как известно, вызывают резкое снижение функции печени и связанная с этим недостаточность других органов, а именно собственный поврежденный альбумин пациента и развитие интенсивной системной воспалительной реакции. Резюме:
Многоцентровое рандомизированное контролируемое исследование для оценки безопасности и эффективности устройства для диализа печени DIALIVE у пациентов с острой хронической печеночной недостаточностью (ACLF) по сравнению со стандартным лечением (SOC). (OA-1997)
Получается VIR предположительно добрался до кзкДНК и генома клетки чтобы заглушить фазу интеграции? Может во второй и третьей фазе наконец то доработают до элиминации HBsAg? Что то последние 2 года тишина по ранее заявленным ARO HBV JNJ и много пабликов про VIR, о котором никто не слышал 2-3 года назад.Существенное снижение HBsAg наблюдалось как у участников HBeAg-, так и у HBeAg + при всех уровнях доз, что позволяет предположить, что VIR-2218 может заглушать транскрипты как кзкДНК, так и интегрированной ДНК. Противовирусная активность VIR-2218, продемонстрированная в этом исследовании, поддерживает дальнейшее развитие в рамках комбинированных схем, направленных на функциональное излечение. Резюме: Безопасность и противовирусная активность VIR-2218, препарата X-нацеленной РНКи, у участников с хронической инфекцией гепатита B: результаты наблюдения 48 недели
 скруджПВТ
скруджПВТ-
kriosan
- Бывалый
- Сообщения: 1578
- Зарегистрирован: 28 окт 2017 17:27
- Пол: ♂
- Гепатит: В
- Генотип: не определял(а)
- Город: Россия
- Благодарил (а): 566 раз
- Поблагодарили: 204 раза
Препараты разрабатываемые против ВГВ
Хорошие новостиScrooge805 писал(а): ↑13 окт 2021 09:20 Существенное снижение HBsAg наблюдалось как у участников HBeAg-, так и у HBeAg + при всех уровнях доз,
