Эффективность индивидуализированной противовирусной терапии хронического гепатита С недостаточно изучена.
Цель. Изучить эффективность противовирусной терапии пэгинтерфероном aльфа 2-а и рибавирином, длительность которой выбирали на основании вирусологического ответа через 4, 8 и 12 недель.
Материал и методы. Первичные пациенты с генотипами 1, 4, 5 и 6 получали лечение пэгинтерфероном aльфа 2-а 180 мкг/нед и рибавирином 1000-1400 мг/сут. Пациентов рандомизировали на группы сравнения через 4, 8 и 12 недель в зависимости от срока клиренса виремии. При наличии быстрого вирусологического ответа (авиремия через 4 недель) противовирусную терапию продолжали в течение 24 или 48 недель. Если клиренс HCV RNA отмечался через 8 недель, длительность лечения составляла 36 или 48 недель. У пациентов с ранним вирусологическим ответом (авиремия или снижение вирусной нагрузки по крайней мере на 2 log через 12 недель) противовирусную терапию проводили в течение 72 или 48 недель. Критерием стойкого вирусологического ответа (СВО) был отрицательный тест на HCV RNA через 24 недели после завершения лечения.
Результаты. 195 из 236 больных, начавших противовирусную терапию, были рандомизированы через 4 (n=50), 8 (n=61) или 12 недель (n=84). У 95% пациентов имелся генотипом 1 HCV. Частота СВО достоверно не отличалась у пациентов, рандомизированных через 4 недели (24-недельный курс – 84%, 48-недельный – 84%), через 8 недель (36-недельный курс – 73%, 48-недельный – 74%) или 12 недель (72-недельный курс – 40%, 48-недельный – 49%). Заключение. У пациентов с генотипом 1 HCV сокращение длительности противовирусной терапии до 24 недель при наличии быстрого вирусологического ответа или до 36 недель при элиминации HCV RNA через 8 недель не привело к снижению частоты СВО по сравнению с 48-недельным курсом лечения. Увеличение длительности противовирусной терапии до 72 недель не сопровождалось более высокой частотой СВО. У пациентов с генотипом 1 HCV и быстрым вирусологическим ответом лечение противовирусными препаратами можно продолжать в течение 24 недель.
Комбинация пэгинтерферона и рибавирина – это стандарт лечения пациентов с хроническим гепатитом С [1]. Вероятность стойкого вирусологического ответа (СВО) самая высокая при быстром клиренсе виремии. У пациентов с генотипом 1 HCV и быстрым вирусологическим ответом (авиремия через 4 недели) сокращение длительности противовирусной терапии до 24 недель не приводит к снижению частоты СВО по сравнению со стандартным 48-недельным курсом лечения [2,3]. Напротив, частота СВО ниже у пациентов, у которых клиренс виремии происходит в более поздние сроки после начала лечения. При отсутствии раннего вирусологического ответа (снижение вирусной нагрузки по крайней мере на 2 log через 12 недель) СВО удается достичь только в отдельных случаях [1]. У пациентов с медленным вирусологическим ответом изучали эффективность 72-недельного курса противовирусной терапии, однако полученные результаты оказались противоречивыми [4-8]. В рандомизированном многоцентровом исследовании IMPROVE изучали эффективность и безопасность индивидуализированной противовирусной терапии пэгинтерфероном aльфа 2-а и рибавирином, подобранной с учетом вирусологического ответа. Первичной целью было сравнение эффективности 72- и 48-недельных курсов противовирусной терапии у пациентов, у которых определялась HCV RNA через 4 и 8 недель, но был достигнут ранний вирусологический ответ через 12 недель. Вторичными целями было сравнение эффективности 24- и 48-недельных курсов противовирусной терапии у пациентов с быстрым вирусологическим ответом, а также 36- и 48-недельных курсов у пациентов, у которых был достигнут клиренс HCV RNA через 8 недель. Материал и методы IMPROVE – это инициированное исследователями, открытое, рандомизированное исследование IIIb фазы, которое проводилось в Канаде в 24 центрах в соответствии с принципами хельсинкской декларации и GCP. Протокол исследования и все поправки были одобрены этическими комитетами лечебных учреждений, а пациенты дали письменное информированное согласие на участие в нем.
Исследование было зарегистрировано под номером NCT00483938 на сайте clinicaltrials.gov. В исследование включали пациентов в возрасте по крайней мере 18 лет с хроническим гепатитом С, у которых определялись антитела к HCV и HCV RNA в сыворотке. Отбирали пациентов с генотипами 1, 4, 5 или 6. Биопсия печени не была обязательным критерием включения. Пациентов с циррозом включали в исследовании при наличии компенсированного заболевания печени (класс А по Чайлд-Пью). У пациентов с циррозом или формирующимся циррозом печени (F3) в течение 2 месяцев до исследования проводили ультразвуковое исследование, компьютерную или магнитно-резонансную томографию и измеряли уровень альфа-фетопротеина (9 л, число тромбоцитов <80*10 9 л и увеличение сывороточного креатинина более чем в 1,8 раза по сравнению с верхней границей нормы, а также беременность и кормление грудью. У женщин репродуктивного возраста критерием включения был отрицательный тест на беременность в течение 24 ч перед введением первой дозы исследуемого препарата. Во время исследования и в течение 6 месяцев после лечения женщинам и партнерам женщин, способных иметь детей, предлагали пользоваться двумя эффективными методами контрацепции.
Во время исследования не допускалось применение системных противовирусных, противоопухолевых или иммуномодулирующих препаратов, включая облучение и системные кортикостероиды. Исследуемые препараты и дизайн исследования Все пациенты получали пэгинтерферон aльфа-2 a (Пегасис) в дозе 180 мкг/нед и рибавирин внутрь два раза в день. Суточную дозу рибавирина подбирали с учетом массы тела: 1000 мг/сут у пациентов с массой тела aльфа 2-а и/или рибавирина в соответствии со стандартной практикой. Дозу рибавирина снижали ступенями по 200 мг. После исчезновения нежелательных явлений дозу разрешалось увеличить до исходной. Во время исследования допускалась монотерапия пэгинтерфероном aльфа 2-а, но не рибавирином. При необходимости исследователи могли применять препараты, стимулирующие эритропоэз. Исходы Сывороточные уровни HCV RNA измеряли с помощью метода Cobas Taqman (порог определения 15 МЕ/мл) исходно и через 1, 2, 4, 8, 12, 24 и 48 недель. У пациентов, получавших 72-недельный курс противовирусной терапии, вирусную нагрузку измеряли также через 72 недели. Первичным критерием эффективности был СВО – авиремия через 24 недели после завершения противовирусной терапии (недели 48, 60, 72 и 96 в зависимости от длительности курса лечения). Рецидивом считали возобновление виремии после завершения противовирусной терапии у пациентов с непосредственным вирусологическим ответом (авиремия в конце курса лечения).
Безопасность Безопасность оценивали на основании нежелательных явлений и частоты снижения доз противовирусных препаратов или прекращения лечения вследствие нежелательных явлений. Особое внимание уделяли следующим нежелательным явления: нейтропения (снижение числа нейтрофилов <0,75*109 л), тромбоцитопения (снижение числа тромбоцитов <50*109 л), анемия (уровень гемоглобина
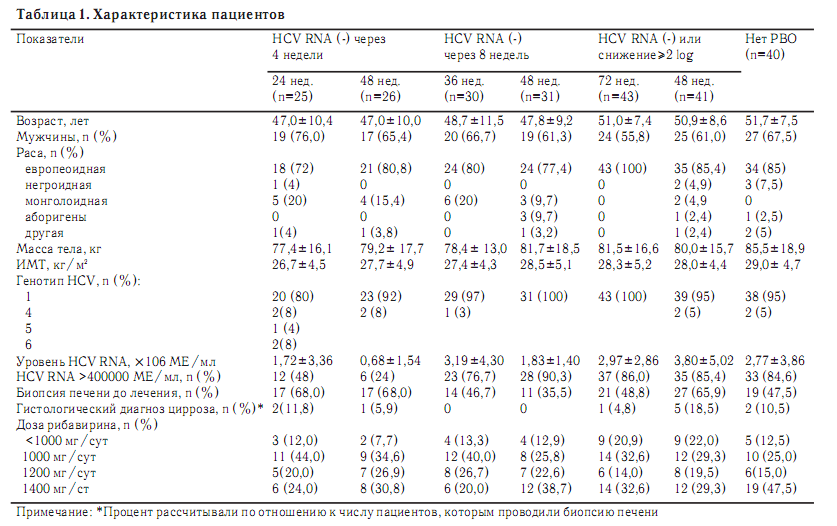
Результаты Исследование было начато 9 июня 2007 года и завершено 7 мая 2010 года. В него были включены 236 пациентов. 196 (83%) из них были рандомизированы на 1 из 6 групп, а 156 (66%) завершили лечение и наблюдение. Среди 80 пациентов, которые не завершили противовирусную терапию, 40 были исключены из исследования в связи с отсутствием вирусологического ответа, 13 отказались от дальнейшего участия в исследовании, 10 выбыли из-под наблюдения, 3 нарушали протокол, 2 умерли и 12 были исключены по другим причинам. Семь из 13 пациентов, отказавшихся от дальнейшего участия в исследовании, были рандомизированы в группу больных, получавших 72-недельный курс противовирусной терапии. Среди 195 пациентов, составивших выборку ITT, быстрый вирусологический ответ был достигнут у 50 (26%) больных, авиремия через 8 недель – у 62 (32%) и ранний вирусологический ответ – у 84 (43%). Исходные показатели пациентов и характеристика проводимой противовирусной терапии приведены в табл. 1 и 2, соответственно. У подавляющего большинства (95%) пациентов имелся генотип 1 HCV. Средняя длительность лечения была близкой к планируемой длительности противовирусной терапии. Исключение составили пациенты, которым проводили 72-недельный курс противовирусной терапии (средняя длительность лечения 60,6 недели). В этой группе только 67% пациентов получили более 80% планируемой дозы пэгинтерферона aльфа 2-а, в то время как в других группах доля таких пациентов составляла по крайней мере 84%.
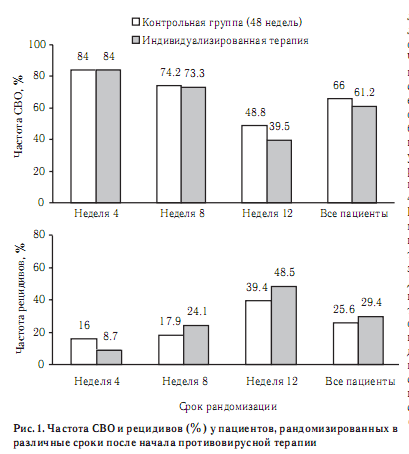
Вирусологический ответ Частота СВО достоверно не отличалась у пациентов с ранним вирусологическим ответом, которые получали 72- или 48-недельные курсы противовирусной терапии (40% и 49%, соответственно; р=0,51; рис. 1).
Частота СВО у пациентов с быстрым вирусологическим ответом, которым проводили 24- или 48-недельную противовирусную терапию, была одинаковой (84%). Достоверной разницы частоты СВО на 36- или 48-недельную противовирусную терапию у пациентов, рандомизированных через 8 недель, также не выявили (73% и 74%, соответственно; р=1,0; рис. 1). Частота СВО у пациентов, которым проводили индивидуализированную противовирусную терапию (61%), была сходной с таковой у пациентов, получавших стандартную 48-недельную противовирусную терапию (66%; р=0,55). Общая частота СВО у всех пациентов, получивших по крайней мере одну дозу исследуемого препарата, составила 53% (124236). Частота рецидивов после индивидуализированной или стандартной противовирусной терапии достоверно не отличалась. Среди 50 пациентов с быстрым вирусологическим ответом HCV RNA не определялась через 1, 2 и 4 недели у 13, 8 и 29 пациентов, соответственно. Рецидив развился только у 1 (5,0%) из 20 завершивших лечение пациентов, у которых авиремия была достигнута через 1 или 2 недели; этот пациент получал 48-недельную противовирусную терапию. Напротив, развитие рецидива наблюдали у 5 (17,9%) из 28 пациентов, у которых клиренс HCV RNA происходил через 2-4 недели после начала лечения. Ранний вирусологический ответ может быть полным (авиремия через 12 недель) или частичным (снижение вирусной нагрузки по крайней мере на 2 log, но сохранение виремии). Каждый тип раннего вирусологического ответа наблюдался у половины из 84 пациентов, рандомизированных через 12 недель. Полный ранний вирусологический ответ был достигнут у 23 (54%) и 19 (46%) пациентов, получавших 72- или 48недельную противовирусную терапию, соответственно, частичный – у 20 (47%) и 22 (54%). Частота СВО на 72и 48-недельную противовирусную терапию составила, соответственно, 52% (1223) и 68% (1319) у пациентов с полным ранним вирусологическим ответом и 32% (722) и 25% (520) у пациентов с частичным ранним вирусологическим ответом. Рибавирин был назначен в дозе 1400 мг/сут 77 пациентам; 58 из них были рандомизированы на 1 из 6 групп. Частота СВО у рандомизированных пациентов составила 66% (3858), в том числе 29% (414) и 58% (712) у пациентов, получавших 72- или 48-недельную противовирусную терапию, 67% (46) и 83% (1012), у пациентов, которым была назначена 36- или 48-недельная терапия, и 100% (66) и 88% (78) у пациентов с быстрым вирусологическим ответом, получавших 24или 48-недельную противовируснуют терапию.
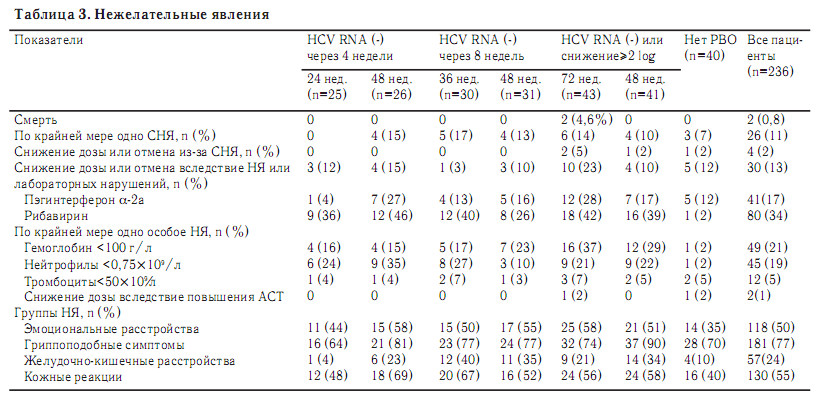
Безопасность Нежелательные явления или отклонения лабораторных показателей были причиной снижения дозы или временного прекращения приема пэгинтерферона aльфа 2-а или рибавирина у 13% и 17% пациентов, соответственно (табл. 3). Чаще всего приходилось снижать дозы или отменять препараты у пациентов, продолжавших лечение в течение 72 недель. Серьезные нежелательные явления отмечались у 26 пациентов, а нежелательные явления, представлявшие особый интерес, – у 80 (34%). В 6 группах частота серьезных нежелательных явлений варьировалась от 10% до 17%, а особых нежелательных явлений – от 26 до 46% (табл. 3).
Явной зависимости частота этих нежелательных явлений от длительности терапии не выявили. Частота выделенных групп нежелательных явлений также не зависела от длительности лечения. Частота анемии была минимальной у пациентов с быстрым вирусологическим ответом и максимальной у пациентов с ранним вирусологическим ответом. Среди пациентов, которым была назначена 48-недельная противовирусная терапия, частота анемии увеличивалась параллельно со сроком рандомизации (15%, 23% и 29% у пациентов, рандомизированных через 4, 8 и 12 недель, соответственно). Напротив, частота нейтропении была максимальной у пациентов с быстрым вирусологическим ответом (29% против 18% и 21% у пациентов, рандомизированных через 8 и 12 недель). Два пациента, которым была назначена 72-недельная противовирусная терапия, умерли. Один случай смерти от внутричерепного кровотечения наблюдали через 2 месяца после введения последней дозы исследуемого препарата. Другой пациент умер от сепсиса через 4 месяца после завершения терапии. Оба случая смерти не связывали с противовирусной терапией.
Обсуждение При первичном анализе не было выявлено разницы частоты СВО на 72- или 48-недельную противовирусную терапию у пациентов, достигших раннего вирусологического ответа через 12 недель. В этих двух группах, против ожидания, была отмечена тенденция к увеличению частоты СВО и снижению частоты рецидивов у пациентов, которым был назначен 48-недельный курс противовирусной терапии. В предыдущих исследованиях, в которых сравнивали 48- и 72-недельную противовирусную терапию у пациентов без быстрого вирусологического ответа, более длительное лечение сопровождалось недостоверным увеличением частоты СВО и снижением частоты рецидивов [5-8]. Причина расхождения полученных результатов остается неясной. Оно могло быть следствием досрочного прекращения более длительной терапии или выхода из-под наблюдения достаточно большого числа пациентов этой группы. В соответствии с принципом intention-to-treat таких пациентов считали не ответившими на противовирусную терапию. Во всех исследованиях у пациентов, которым назначали 72-недельную противовирусную терапию, была выше частота досрочного прекращения лечения [4-8]. Частота СВО была сходной у пациентов с быстрым вирусологическим ответом, которым проводили 24или 48-недельную противовирусную терапию. Сходная частота СВО была также отмечена при проведении 36- или 48-недельной противовирусной терапии у пациентов, у которых клиренс HCV RNA происходил через 8 недель. Ни в одном из предыдущих исследований не изучали эффективность сокращенного курса противовирусной терапии у пациентов с вирусологическим ответом через 8 недель. Общая частота СВО у таких больных была очень высокой (около 74%) и значительно превышала таковую у пациентов, рандомизированных через 12 недель (<50%). В других исследованиях у пациентов с генотипом 1 HCV, в которых длительность противовирусной терапии выбирали с учетом вирусологического ответа через 8 недель, также была отмечена высокая частота СВО. Например, в исследовании Mangia и соавт. частота СВО у таких пациентов, получавших стандартную или индивидуализированную противовирусную терапию, составила 70% и 72%, соответственно [6].
К сожалению, в этом исследовании, всем пациентов с вирусологическим ответом, достигнутым через 8 недель, проводили 48-недельную противовирусную терапию, поэтому полученные данные не позволяют судить о возможности сокращения курса лечения при наличии авиремии через 8 недель. Относительное небольшое число пациентов в этой подгруппе в настоящем исследовании не позволяет исключить ошибку II типа, однако следует отметить соответствие частоты СВО в когорте пациентов с вирусологическим ответом через 8 недель, которым проводили 48-недельную терапию, и в более крупной когорте в исследовании Mangia и соавт. [6]. Общая частота СВО была сопоставимой у пациентов, получавших индивидуализированную и стандартную 48-недельную противовирусную терапию, что согласуется с результатами предыдущих исследованиях [6,9]. Соответственно, внедрение в клиническую практику сокращенных 24и 36-недельных курсов лечения позволит сократить затраты на противовирусную терапию. В настоящее время возрастает интерес к очень ранней кинетике вирусной нагрузке (до 4 недель) как к показателю возможного ответа на терапию. В настоящем и предыдущих исследованиях было показано, что чем быстрее происходит элиминация HCV RNA в течение первого месяца, тем выше вероятность СВО [10,11]. Элиминация виремии в течение 1 или 2 недель сопровождалась значительным снижением частоты рецидивов HCV-инфекции по сравнению с таковой у пациентов, у которых HCV RNA переставала определяться через 4 недели. Каково значение результатов настоящего исследования в эру противовирусных препаратов прямого действия? В ближайшем будущем в большинстве стран мира будут зарегистрированы первые подобные препараты – ингибиторы протеазы HCV. Тем не менее, комбинация пэгинтерферона и рибавирина сохранит важное значение в лечении HCV-инфекции, так как ингибиторы протеазы необходимо применять в сочетании со стандартными средствами для профилактики резистентности. Кроме того, тройная противовирусная терапия вызывает побочные эффекты чаще, чем стандартная [12-14]. Соответственно, у некоторых пациентов, которые не переносят ингибиторы протеазы, придется проводить двойную терапию. И наконец, подавляющее большинство из 180 млн HCV-инфицированных проживают в развивающихся странах, таких как Египет, Пакистан и Монголия [15]. В этих регионах высокая стоимость противовирусных препаратов прямого действия будет препятствовать назначению тройной противовирусной терапии (исключая пациентов, не ответивших на интерферон и рибавирин). Следовательно, результаты проведенного исследования найдут применение во многих регионах мира, в которых двойная комбинированная терапия останется стандартом на протяжении многих лет. Производители частично оправдывают высокую стоимость первых препаратов прямого действия возможностью сокращения общей длительности лечения. Однако они продолжают настаивать, что длительность двойной противовирусной терапии должна составлять 48 недель. Результаты настоящего и предыдущих исследований [2,3,6,9] доказали, что у пациентов с генотипом 1 при наличии быстрого вирусологического ответа можно сократить длительность противовирусной терапии до 24 недель. Хотя частота быстрого вирусологического ответа у американцев с генотипом 1, получавших двойную противовирусную терапию, была достаточно низкой (примерно 8-11%) [12-14], в настоящем исследовании, которое проводилось в Канаде, она достигла 21%, а в итальянском многоцентровом исследовании – 27% [6]. В регистрационных исследованиях пэгинтерферона aльфа 2-а и рибавирина частота быстрого вирусологического ответа у 1383 пациентов с генотипом 1 составила 16% [16], а в Тайване – 44% [9]. При анализе эффективности затрат на дорогостоящую тройную противовирусную терапию необходимо учитывать вариабельность частоты быстрого вирусологического ответа на двойную терапию и рассчитывать затраты на сокращенный 24недельный курс лечения у таких пациентов. В некоторых регионах, в которых отмечается достаточно высокая частота быстрого вирусологического ответа, имеет смысл начинать лечение с вводной 4-недельной терапии двумя препаратами и добавлять дорогостоящий ингибитор протеазы только при отсутствии быстрого вирусологического ответа. При наличии быстрого ответа целесообразно проводить 24-недельную двойную противовирусную терапию, что позволит значительно снизить затраты и риск нежелательных эффектов. Проведенное исследование имеет ряд ограничений. Число пациентов, включенных в исследование, оказалось ниже запланированного, что снижает статистическую силу анализа. Кроме того, роль генотипа ИЛ-28B как предиктора ответа на лечение была описана недавно [17,18], поэтому его не анализировали во время исследования. Дисбаланс генетического полиморфизма в группах сравнения может оказать значительное влияние на эффективность лечения, особенно в небольших рандомизированных исследованиях, поэтому в будущих исследованиях необходимо стратифицировать пациентов с учетом этого фактора. Таким образом, результаты рандомизированного исследования у пациентов в основном с генотипом 1 показали, что сокращение длительности противовирусной терапии до 36 недель при наличии вирусологического ответа через 8 недель не приводит к снижению частоты СВО по сравнению с таковой при стандартной 48-недельной терапии. Авиремия через 8 недель может быть полезным показателем для индивидуализации противовирусной терапии. Исследование также подтвердило, что при наличии быстрого вирусологического ответа у пациентов с генотипом 1 лечение можно продолжать в течение 24 недель. Эта парадигма сохраняет значение в эру противовирусных препаратов прямого действия.
Литература
1. Ghany MG, Strader DB, Thomas DL, Seeff LB. Diagnosis, management, and treatment of hepatitis C: an update. Hepatology 2009; 49: 1335–74. 2. Jensen DM, Morgan TR, Marcellin P, et al. Early identification of HCV genotype 1 patients responding to 24 weeks peginterferon alpha-2a (40 kd) ribavirin therapy. Hepatology 2006; 43: 954–60. 3. Zeuzem S, Buti M, Ferenci P, et al. Efficacy of 24 weeks treatment with peginterferon alfa-2b plus ribavirin in patients with chronic hepatitis C infected with genotype 1 and low pretreatment viremia. J Hepatol 2006; 44: 97–103. 4. Berg T, von WM, Nasser S, et al. Extended treatment duration for hepatitis C virus type 1: comparing 48 versus 72 weeks of peginterferon-alfa-2a plus ribavirin. Gastroenterology 2006; 130: 1086–97. 5. Sanchez-Tapias JM, Diago M, Escartin P, et al. Peginterferon-alfa2a plus ribavirin for 48 versus 72 weeks in patients with detectable hepatitis C virus RNA at week 4 of treatment. Gastroenterology 2006; 131: 451–60. 6. Mangia A, Minerva N, Bacca D, et al. Individualised treatment duration for hepatitis C genotype 1 patients: a randomized controlled trial. Hepatology 2008; 47: 43–50. 7. Buti M, Lurie Y, Zakharova NG, et al. Randomized trial of peginterferon alfa- 2b and ribavirin for 48 or 72 weeks in patients with hepatitis C virus genotype 1 and slow virologic response. Hepatology 2010; 52: 1201–7. 8. Ferenci P, Laferl H, Scherzer TM, et al. Peginterferon alfa-2a ribavirin for 48 or 72 weeks in hepatitis C genotypes 1 and 4 patients with slow virologic response. Gastroenterology 2010; 138: 503–12. 9. Yu ML, Dai CY, Huang JF, et al. Rapid virological response and treatment duration for chronic hepatitis C genotype 1 patients: a randomized trial. Hepatology 2008; 47: 1884–93. 10. Neumann AU, Bain VG, Yoshida EM, Patel K, Pulkstenis E, Subramanian GM. Early prediction of sustained virological response at day 3 of treatment with albinterferon-alpha-2b in patients with genotype 2 3 chronic hepatitis C. Liver Int 2009; 29: 1350–5. 11. Neumann AU, Pianko S, Zeuzem S, et al. Positive and negative prediction of sustained virologic response at weeks 2 and 4 of treatment with albinterferon alfa-2b or peginterferon alfa-2a in treatment-naive patients with genotype 1, chronic hepatitis C. J Hepatol 2009; 51: 21–8. 12. Hezode C, Forestier N, Dusheiko G, et al. Telaprevir and peginterferon with or without ribavirin for chronic HCV infection. N Engl J Med 2009; 360: 1839–50. 13. McHutchison JG, Lawitz EJ, Shiffman ML, et al. Peginterferon alfa-2b or alfa-2a with ribavirin for treatment of hepatitis C infection. N Engl J Med 2009; 361: 580–93. 14. Kwo PY, Lawitz EJ, McCone J, et al. Efficacy of boceprevir, an NS3 protease inhibitor, in combination with peginterferon alfa-2b and ribavirin in treatment naive patients with genotype 1 hepatitis C infection (SPRINT-1): an open-label, randomised, multicentre phase 2 trial. Lancet 2010; 376: 705–16. 15. Lavanchy D. The global burden of hepatitis C. Liver Int 2009; 29(Suppl 1): 74–81. 16. Fried MW, Hadziyannis SJ, Shiffman ML, Messinger D, Zeuzem S. Rapid virological response is the most important predictor of sustained virological response across genotypes in patients with chronic hepatitis C virus infection. J Hepatol 2011; 55: 69–75. 17. Ge D, Fellay J, Thompson AJ, et al. Genetic variation in IL28B predicts hepatitis C treatment-induced viral clearance. Nature 2009; 461: 399–401. 18. Suppiah V, Moldovan M, Ahlenstiel G, et al. IL28B is associated with response to chronic hepatitis C interferon-alpha and ribavirin therapy. Nat Genet 2009; 41: 1100–4.


